In questi giorni mi sono arrivati molti messaggi di lettori afflitti da dubbi esistenziali sul pH di mash. Tutto è nato a valle di un post che ho pubblicato qualche giorno fa, a sua volta ispirato da un articolo apparso sul numero di Dicembre di Brew Your Own.
Il tema toccato da Mr Wizard in quell’articolo è lo stesso affrontato diverso tempo fa da Kai Troester, meglio noto come Braukaiser. Il post di Braukaiser, pubblicato addirittura nel 2011, sottolinea le incongruenze presenti nella letteratura birraria relativamente al range ottimale del pH di mash. Per tranquillizzare anzitutto me stesso, sono andato a studiarmi un po’ di materiale sul tema. Espongo in questo post i miei ragionamenti e le conclusioni a cui sono arrivato. Sempre disponibile a essere eventualmente smentito da chi ne sa più di me.
Partiamo da un assunto fondamentale:
VARIABILITÀ DEL PH CON LA TEMPERATURA
Il pH misura la concentrazione degli ioni idrogeno in una soluzione. La scala va da 0 a 14. A pH=14 si ha la minima concentrazione di ioni idrogeno e fino a pH=7 la soluzione si definisce basica (o alcalina). A pH=7 la soluzione è neutra. Tra 7 e 0 la soluzione è acida e a pH=0 si ha la massima concentrazione di ioni idrogeno nella soluzione (una mole per litro).
Back to some basic chemistry today, with a look at the pH scale: http://t.co/mIjnKEAlye pic.twitter.com/zd8G6nxb3X
— Compound Interest (@compoundchem) 9 luglio 2015
Queste definizioni si intendono valide alla temperatura di riferimento di 25°C. Vediamo perché questa temperatura è così importante.
L’acqua distillata a temperatura ambiente ha un pH pari a 7 e si trova nella condizione di equilibrio descritta dalla reazione di autoionizzazione dell’acqua. Quando viene applicato calore (heat) la reazione si sposta verso destra rilasciando ioni idrogeno (che si legano alle molecole di acqua formando H3O+) fino a quando non si torna nuovamente in equilibrio.
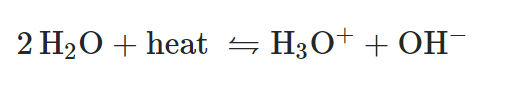
La maggiore concentrazione di ioni idrogeno fa diminuire il pH dell’acqua (vedi tabella sopra). Dal grafico seguente si evince chiaramente come il pH dell’acqua distillata, e quindi di qualsiasi soluzione acquosa con andamenti diversi, vari al variare della temperatura.
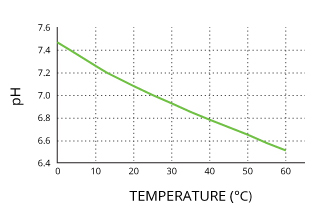
Ciò non significa però che riscaldando l’acqua questa diventi più acida. Con l’aumentare della temperatura aumenta la concentrazione degli ioni idrogeno, ma al contempo sale anche la concentrazione degli ioni OH-. La neutralità di una soluzione non si definisce in base alla concentrazione degli ioni idrogeno ma in base alla differenza di concentrazione tra questi (cationi) e gli ioni OH- (anioni). Applicando calore aumenta la concentrazione di entrambi in egual misura, quindi la soluzione rimane neutra ma il pH varia (perché varia la concentrazione degli ioni).

Alla temperatura di 90°C, per esempio, il pH dell’acqua distillata scende a 6.07 ma il rapporto tra anioni e cationi rimane 1:1. Possiamo quindi affermare che l’acqua distillata a 100°C ha un pH neutro pari a 6.07, mentre a 25°C il suo pH neutro è 7.
Capite ora quanto è importante citare la temperatura di riferimento insieme al valore del pH?
La variazione del pH con la temperatura è molto più contenuta nelle soluzioni acide, mentre è più marcata nelle soluzioni basiche, come si evince dalla tabella seguente.

Ma torniamo al pH della birra e in particolare a quello di mash.
PH DI MASH
La confusione nei valori di riferimento del pH di mash nasce dalla ambiguità delle tabelle citate nella letteratura birraria. È stato empiricamente dimostrato che il pH di mash è minore di quello misurato a temperatura ambiente di circa 0.3 unità (sappiamo che il pH di qualsiasi soluzione acquosa diminuisce con l’aumentare della temperatura). Quello che non risulta chiaro, però, è quale sia la temperatura di riferimento dei valori di pH che troviamo in letteratura. Partendo dall’articolo di Braukaiser segnalato sopra e integrandolo con altre fonti (citate nelle note) ho costruito la seguente tabellina.
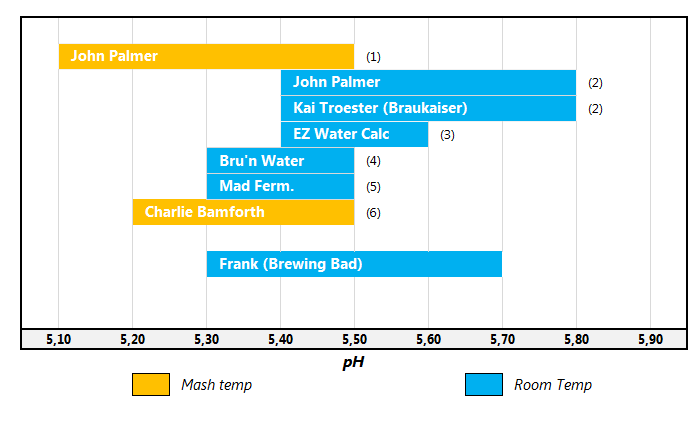
Fonti:
- John Palmer
- Braukaiser cita John Palmer
- EZ Water Calculator
- Bru’n Water Spreadsheet
- The Mad Fermentationist (non è un range ma il suo pH preferito per la produzione di APA)
- Charles Bamforth
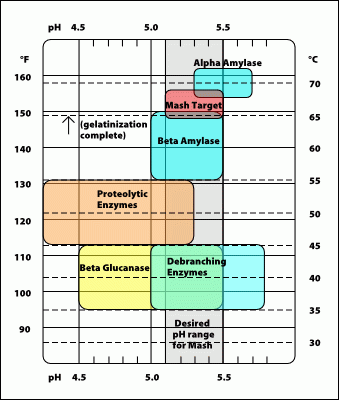
Nella tabellina sotto vengono indicati i valori di pH ottimali per i vari enzimi (Charles Bamforth, fonte n.6)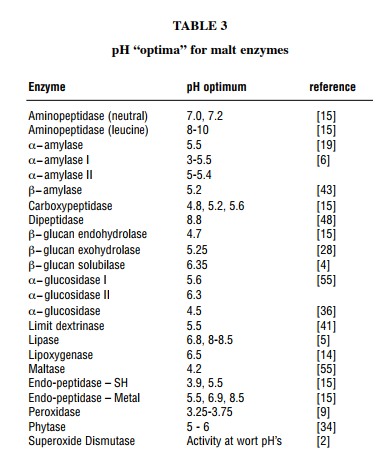
Alla fine risulta abbastanza evidente come nella letteratura birraria si sia fatta un po’ di confusione tra i pH misurati a temperatura ambiente e quelli di lavoro degli enzimi citati nella lettura scientifica. Per esempio, Bamforth indica per la alfa amilasi il valore pH=5.5 che coincide con l’estremo del range indicato da Palmer se misurato a 25°C (5.5.+0.3=5.8).
Personalmente mi muovo più o meno in linea con il range proposto da Kai Troester e Palmer, ovvero tra pH 5.3 e 5.7 misurato a 25°C.
PERCHÈ MISURARE IL PH A 25°C?
Alla luce di quanto detto, mi vengono in mente almeno tre ragioni:
- per coerenza con la neutralità del pH=7 che è valida solo a temperatura ambiente
- per mantenere la coerenza del valore misurato lungo tutta la catena di produzione, a prescindere dalle variazioni di temperatura del mosto/birra
- per preservare la sonda dei pH meter che soffre temperature troppo alte.
E LA CORREZIONE AUTOMATICA DEL PH?
La compensazione automatica dei pH meter non c’entra nulla con la variabilità del pH in funzione della temperatura.
Ma proprio nulla.
Le sonde dei pH meter generano una corrente proporzionale alla concentrazione degli ioni idrogeno. La conducibilità della sonda e quindi la corrente generata varia con la temperatura. Il valore del pH viene calcolato in base a una formula matematica che si muove lungo una retta la cui pendenza varia anch’essa con la temperatura.
Per dirla semplice: anche se il pH della soluzione rimanesse stabile al variare della temperatura, la sonda leggerebbe un valore di corrente (e quindi di pH) diverso.
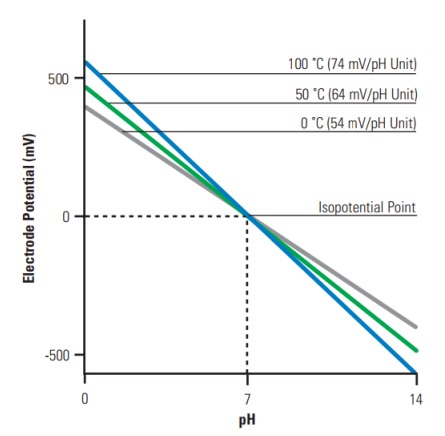
Facendo partire per esempio una linea retta dal valore di 400mV nel grafico sopra si incrociano le tre rette in tre punti diversi, corrispondenti a 3 valori diversi di pH. Solo scegliendo la giusta pendenza (ovvero conoscendo la temperatura della misura) si otterrà il valore di pH corretto.
La correzione della temperatura è quindi essenziale se non si fa lavorare la sonda alla temperatura per cui è stata impostata la formula matematica nel lettore di pH.
I pH meter con ATC (Automatic Temperature Compensation) hanno una sonda di temperatura incorporata che rileva la temperatura e sceglie automaticamente la correzione opportuna (ovvero sceglie la retta giusta per calcolare il pH). Altri pH meter vengono forniti con una tabellina che permette di compensare manualmente la lettura del pH in base alla temperatura di misura.
CONCLUSIONI
Riassumo brevemente i punti salienti dell’articolo, ovvero i concetti chiave da portare a casa:
- il pH di una soluzione diminuisce all’aumentare della temperatura. Il tasso di diminuzione dipende dalla composizione della soluzione
- il pH di mash (misurato intorno ai 67°C) è minore di 0.3 rispetto alla stessa misura operata a temperatura ambiente (25°C)
- il range ottimale del pH di mash per gli enzimi varia tra 5.3 e 5.7 (misurato a 25°C)
- nella parte bassa del range si favorisce la beta amilasi, nella parte alta la alfa amilasi
- misurando sempre il pH a temperatura ambiente (25°C) si ottengono misure confrontabili durante tutto il processo di produzione
- misurando sempre il pH a temperatura ambiente (25°C) si preserva il funzionamento della sonda del pH meter
- la compensazione di temperatura del pH meter (ATC) compensa l’offset della sonda ed è obbligatoria se si misura il pH lontano dal range di funzionamento della stessa (in genere temperatura ambiente)
- la compensazione di temperatura del pH meter (ATC) non tiene conto della variabilità del pH della soluzione con la temperatura. Questa dipende dalla composizione della soluzione.
Se ho scritto minchiate, vi prego si segnalarle nei commenti. Spero comunque di aver fatto un po’ di chiarezza.





Articolo Illuminante, chiaro come pochi. Grazie mille!!!
È stato utile anche per me! 🙂
Ciao Frank, ma la temperatura ambiente non era 20 gradi?
Io non mi fido più del pH Meter sono passato alle cartine tornasole.
Ma il mash e caldo tempo che raffreddi il campione e l’attività enzimatica nel mash mica ti aspetta.
Io sono lì che aggiungo acido per abbassarlo ma niente poi ne aggiungo ancora un po’ ed ecco il danno pH troppo basso.
Io poi acidificò anche l’ acqua di sparg ma dice certamente non se serve.
Insomma ho ancora mille dubbi pratici sul PH
Con le cartine tornasole è davvero difficile distinguere i colori nel range di ph 5-6. Ti consiglio di prepararti con delle tazzine o tazze in ceramica messe nel congelatore, poi prelevi il mosto caldo con una tazza a temperatura ambiente, lo fai freddare leggermente, poi lo passi in quelle prese dal congelatore e in 2 minuti sei a 20-30°C (se sei nel range va bene lo stesso, il pH non cambia così tanto nel giro di 10°C). Il campione che serve è ridotto, si fredda in pochissimo nelle tazzine conngelate.
Ciao Frank, articolo approfondito come al solito, grazie.
Di solito io misuro con PHmetro “cinese” dopo il mash-in a 45°, cerco di tenermi tra i 5.5 e 5.8 perche’ “mi e’ sempre sembrato giusto”. Ora so perche’.
Auguri !
Eh, ma non mi pare giusto. Dovrebbe essere un po’ più basso (diciamo che sei a metà tra T ambiente e T di mash, ma 5.8 mi pare troppo). A ogni modo, perché non freddare il campione? Lo sto dicendo a tutti perché mi pare assurdo non farlo visto che servono meno di 100ml per la misura e si raffreddano in un attimo versandoli in un pentolino tenuto in congelatore.
In effetti, forse mi sono spiegato male, o non mi sono spiegato affatto :-).
Misuro dopo mash-in a 45° appunto per lasciare il tempo di acidificare, raffreddo un campione e misuro. I phmetri cinesi, anche ATC, ci mettono una vita a “termoregolarizzarsi”, anche 5′ a volte.
Quindi, campione temperatura ambiente (di solito messo in un bel bicchierotto di vetro), e via di misura, in 30” e’ fatta. Poi, colla T piu’ alta il PH scende…. o mi confondo io ????
Ma fai sempre mash-in a 45°C? Come mai? Comunque purtroppo continuo a non seguirti… 🙂 Prima parli di 5 minuti, poi 30 secondi… non capisco.
Si, per il 90% delle volte faccio mash-in a 45°, perche’ uso spesso malto base pilsener e acqua calda sanitaria (passata per addolcitore) dell’ impianto di casa tarato a 50°. Aggiungendo il malto, arrivo a 45-47°. Tempo fa mettevo il PHmetro ATC direttamente dentro al mash. Da manuale lo strumento corregge solo fino a 50°, ma per raggiungere solo i 45° da temperatura ambiente ci metteva anche 5′. Ora prelevo un campione, lo metto in un bicchiere pre-raffreddato, mischio e il tutto si assesta a 25-30°, temperatura che il PHmetro raggiunge in 30”. Portato il mash a PH diciamo, 5.5 circa con acido lattico, faccio 10′ di pausa a 52°, poi a 67° so’ che il PH scendera’ a 5.2 circa. Spero di essermi spiegato 🙂
Che dire, spiegazione cristallina!
L’unica cosa che mi fa imbestialire con il ph è come esso varia a seconda di quando viene misurato durante la fase di mash. Personalmente mi trovo variazioni importanti se misurato a 10, 30 o 60 min dopo il mash (o sono solo io?)
Pertanto a mio parere anche questo comporta un margine di errore.. sbaglio?
Il pH varia durante il mash, anche perché in bollitura arriva con un valore più basso. Credo però che la maggior parte dell’attività enzimatica avvenga nella prima mezz’ora del mash, quindi il calo influisce relativamente.
Decisamente esaustivo, ben fatto. Resta quindi soltanto il problema di capire con CERTEZZA a che cavolo di temperatura si riferiscono i testi, a questo punto farò anche io delle ricerche in merito.
Per mera correttezza formale (e non di concetto) H30+ prende il nome di ione ossonio (ed è un catione) e OH- ione idrossido (ed è un anione).
Per una ancora più incontrovertibile evidenza da nerd, quando parli dell’acqua distillata e della variazione del pH: la neutralità di una soluzione non dipende dalla sola concentrazione dello ione ossonio, ma dalle concentrazioni di ossonio e idrossido rispetto al prodotto ionico dell’acqua, che varia con la temperatura. Di conseguenza il pH, che misura la concentrazione dello ione ossonio, varia con la temperatura ma le proporzioni di ossonio e irossido restano immutate, da qui la neutralità dell’acqua distillata a ogni temperatura.
L’acqua distillata a 100° dovrebbe avere pH 6,14 (fonte: https://goo.gl/Ttexv6)
Grazie del chiarimento “nerdoso”. 🙂 poi correggo anioni e cationi e scrive solo ioni va ah ah
Bell’articolo, tutto esplicato con grande cognizione di causa …
Un solo grande dubbio permane ancora … correggetemi se dico mischiate ma sulla base di tutto ciò il ph target da leggere con ph metro atc a temperatura 25 C° sarebbe 5.6-5.7 per un ph di mash target di 5.3/5.4 …. ph non troppo lontano da quello ottenuto senza uso di malti acidi o acido lattico … allora correggere non è necessario ? Il dubbio permane …
Bè, il ph a cui si stabilizza il mash dipende dai bicarbonati presenti nell’acqua. Con bicarbonati a 200ppm nelle birre chiare si stabilizza a valori decisamente più alti. Poi 5.8 è il limite, di solito si lavora intorno a 5.5 misurato a T ambiente ed è difficile arrivarci senza il supporto di acidi anche con bicarbonati bassi.
Qualche mese fa mi sono imbattuto in un articolo di Ashton Lewis (credo proprio postato da te su Facebook, ma non ricordo con certezza) che mi aveva fatto passare la voglia di correggere l’acqua proprio perché metteva in crisi una delle poche certezze che avevo, e cioè che il range 5.2-5.5 fosse da intendersi a temperatura ambiente:
«The rule of thumb pH range of 5.2–5.5 is the pH of the actual hot mash, not the cooled sample. This means that the temperature-corrected pH is about 0.35 units higher, or pH 5.55–5.85. It is really best to use pH meters without automatic temperature compensation (ATC) because the ATC only accounts for the difference in how the electrode output voltage is affected by temperature and if you use the output from a temperature-corrected pH the result is confusing to compare to data published in the brewing literature.»
Considerando la fonte affidabile mi sono messo a seguirla con un atto di fede. Adesso che hai spiegato come il pH varia in base alla temperatura, so anche il perché e posso continuare a correggere l’acqua con più cognizione di causa. Perciò, ancora una volta, grazie per il tuo lavoro! 😉
In sostanza avendo un phametro atc,mi consigli di misurare a 25gradi,e di nin fare nessuna correzione?prendo per buono il valore letto a quella temperatura giusto?
È esattamente quello che ho scritto nel post.:-) (e quello che faccio io)
Boom… mi hai aperto il cervello caro frank. Bellissimo articolo, chiaro e utile. Risolve problemi che birrificatori “quaquaraqua” come me non sanno nemmeno di avere. Oggi mi hai reso un homebrewer migliore 🔝
Mi fa estremamente piacere!
Grazie Frank per un altro articolo rigorosamente scientifico, su un argomento molto discusso.
Approfitto dell’argomento per chiederti il tuo parere sulla misurazione del PH nell’acqua di sparge.
Alcuni si preoccupano del PH di Sparge , motivando che , un corretto valore , riduce l’estrazione di tannini e facilita l’estrazione degli ‘zuccheri’ residui durante il lavaggio. Cosa ne pensi ?
Facendo BIAB (a volte con un piccolissimo sparge) non mi curo dell’acqua di sparge (sciacquo le trebbie con un paio di bottiglie di acqua panna a temperatura ambiente giusto per facilitare lo “sgocciolamento”). In genere però l’estrazione dei tannini è molto influenzata dal pH (maggiore è il pH, più intensa l’estrazione) e se lo sparge è significativo potrebbe influire (molto più della temperatura alta). Bisogna però tenere anche da conto che l’acqua, una volta entrata nel letto dei grani, si diluisce con un fluido già di per se’ acido visto che il pH dei grani durante il mash scende fino a 5.2. In estrema sintesi: una aggiustata è bene dargliela, ma è sufficiente portare il pH intorno a 6. Ovviamente, da BIABista, parlo esclusivamente dal punto di vista teorico perché che non ho grande esperienza di sparge (ho fatto un po’ di sparge nelle prime cotte, ma non ero così esperto da poter valutare bene la questione).
Confermo che anch’io porto sempre l’acqua di sparge su PH 6, in linea con quanto ho letto spesso in giro. Per chi usa il solfato di calcio: occhio che con l’acqua di sparge non funziona… ma questa è un’altra storia 🙂
Ciao Frank ti seguo spesso e con grande entusiasmo anche perché focalizzi nei tuoi articoli grandi verità da cui attingere esperienza nel prodursi birra in casa.
Mi reputo ancora un neofita anche se ora seguendo un corso serio e facendo anche una fase pratica in birrificio sto imparando tanto il mio insegnante è un ingegnere della birra tedesco che continua ad imparare e innovarsi sempre .Senza dilungarmi tanto fuori argomento il mash da un po’ di tempo è cambiato pure da parte mia stabilizzato il pH a temperatura ambiente non modifico nulla accendo i fuochi e faccio andare la temperatura fino a quando metto i malti per iniziare il mash così che vuoi alzamento temperatura vuoi introduzione malti il pH cambia diminuisce…ad una base di 5,7-5,8 a quel punto scoperto il malto acidulo macino la quantità corrispondente all’1% di ciò che ho messo in infusione ed abbasso al range di pH 5,4 il valore da tutti stimato come media…e va da solo
Grazie per tutte le tue condivisioni su un argomento che mi ha preso davvero a cuore come questo bellissimo alimento…
Ciao Frank, scusami ma io sono un po stupido e per essere certo di quello che faccio voglio farti questa stupida domanda (giusto per essere sicuro di aver capito)
Se io voglio favorire la b-amilasi devo avere un ph di 5.2/5.3 in pentola e quindi di 5.5/5.6 misurato a temperatura ambiente giusto?
Yes
Ciao Frank, seguo da molto il tuo blog e questo è uno dei tuoi migliori articoli, ottimo il contenuto e ottima le spiegazione. Bravo.
Grazie!
Gordon Strong, tanto per dare un altro dato, predilige un PH più basso. Lui porta l’acqua a PH 5.5 (misurato a 20°C) così che durante il mash, con i grani, arriva a 5.1-5.3.
(cfr. “Modern homebrew recipes”, cap.1)
Scusa Francesco ma il valore di ph che viene fuori x esempio da Bru’n Water, si intende a temperatura di mash o a temperatura ambiente?
Temperatura ambiente (è scritto espressamente nel testo del foglio di calcolo per il grain bill). Nel grafico che ho fatto sopra infatti ho messo il range di Bru’n Water in blu (Room Temp).
Quindi in pratica se voglio misurare con atc a 25gradi ptendo per buono quello che mi da’ ,e se invece.la temp. Del campione da misurare sia piu’bassa o piu’alta.devo fare.sempre una correzione?ovvero se misuro ph a 40gradi e mi da 5.8 in realta’ho 5.5? Se invece misuro ph a 15gradi e mi da ph 5.7 vuol dire che ho ph reale di 5.4? Con temperature maggiori o minori applico una correzione di 0,3 o sbaglio?
Ciao Matteo, è tutto scritto nel post. Se lo rileggi con un attimo di calma, avrai tutte le risposte alla tua domanda (perdonami, ma non posso rimettermi a scrivere qui quello che ho già scritto sopra). Se poi qualcosa nello specifico non è chiaro, chiedi pure.
Domanda idiota: nell’ottica di far birra con meno seghe mentali possibili, una volta che uno ha calcolato il PH con un foglio di calcolo (sul quale riporta le aggiunte di sali e anche i malti usati -che ovviamente contribuiscono a variare il PH), ha senso misurare il PH durante la birrificazione, o ci si può fidare? Se è meglio misurarlo, perché?
No, va misurato. Giusto se facessi sempre la stessa ricetti e fossi sicuro che le analisi della tua acqua sono rimaste invariate potresti in teoria non misurare. Ma è sempre meglio misurare.
Grazie Frank dell’articolo utile ed esplicativo: della serie “nerd” volevo dire per completezza che l’acqua distillata in equilibrio con l’atmosfera (cioè dopo un po’ di tempo che è stata “prodotta”) assesta il suo pH intorno a 5,6 a causa del discioglimento nell’acqua di CO2 atmosferica per la legge di Henry: l’acido carbonico che si forma abbassa infatti il pH. (da questo derivano i saponi a pH “neutro”! 5.5).
I sali disciolti in genere riportano questo valore, per l’acqua potabile, intorno alla neutralità.
Io ho difficoltà nella taratura del mio pHametro (come del resto la avevo quando ho fatto una tesi di laurea sulle “piogge acide”).
Mi sto orientando perciò sull’utilizzo di cartine indicatrici per controllare il ph di mash anche se ancora non ho trovato quelle specifiche di intervallo 5-6 più precise della generica “tornasole”.
Spero di non essermi reso antipatico con la “nerdata” ma ti saluto e ti ringrazio per i tuoi utili articoli.
Grazie per la precisazione. Le cartine per la mia esperienza sono troppo approssimative perchè le differenze di colore tra ph 5.5 e 5.8 sono impercettibili. Investi in un milwaukee mw101 e non avrai più problemi di taratura.
Hola Frank. è possibile che tutte le volte che correggo l’acqua di mash prima di mettere i grani, la lettura del phmetro ( a 23 gradi dopo 10 minuti che ho iniziato il mash) mi da 5,2-5,3 e, dopo mezz’ora e un’ora me lo ritrovo a 5,6-5,7? Non dovrebbe essere al contrario? la mia acqua ha 100 ppm di bicarbonati.
Grazie.
Davide
Il pH è sempre meglio leggerlo e correggerlo dopo il mash in, non prima. Non so perchè nel tuo caso risale, ma ti consiglio di fare mashin, leggere ed eventualmente correggere.
Si,perdonami. Non mi sono spiegato bene. Aggiungo i sali, aggiungo i grani, aspetto 10 minuti e leggo. a temperatura ambiente la prima misura mi da intorno a 5,2-5,5, dipendendo da quello che sto cercando. Dopo 30 minuti il ph si alza sempre di 0,3. Per acidificare l’acqua di mash uso acido citrico. Sarà quello? Forse non fa abbastanza effetto tampone avendo i bicarbonati a 100 ppm? Magari col fosforico, avrei un maggior effetto?
Un’ altra domanda: leggendo il libro di Strong dice di aggiungere i sali in bollitura, non nella pentola di liquore. Lo hai mai provato?
Grazie
Davide
Ciao Frank!
Per la tua esperienza è più preciso ez water calculator o BeerSmith per il calcolo dell’ acido lattico da mettere?
Poi ti chiedo se anche a te succede che, per esempio, ez water calculator ti calcola 2ml per arrivare al ph desiserato ma poi in realtà lo ottieni con 1,5 ml?
Non saprei, non ho mai usato il tool interno di Beersmith per correggere l’acqua. A ogni modo, piccole variazioni nei dosaggi sono comuni, anche semplicemente per la variabilità stagionale dei valori dell’acqua, che sia di rete o di fonte.
Si ma quindi consigli di fare il mash-in a 25 gradi ?
in che senso? Mica ho capito…
Se voglio misurare il ph a 25 gradi devo comunque prima inserire i grani e poi procedere con la lettura giusto ? quindi il mash-in inevitabilmente andrà fatto a 25 gradi
Direi di no. Per misurare il pH a 25°C prendi un campione del mosto (senza grani né glumelle) alla temperatura in cui stai facendo il mash, dopo circa dieci minuti dal mashin, lo freddi fino a 25°C (ci vuole poco mosto, quindi freddarlo è facile e veloce) e misuri il pH.
Ciao Frank, tu scrivi “il range ottimale del pH di mash per gli enzimi varia tra 5.3 e 5.7 (misurato a 25°C)”:
quindi ti chiedo è consigliato abbassarlo sempre il pH? per qualsiasi stile ci approntiamo a fare?
Le ultime 2 birre che ho provato a fare in BIAB ho acidificato con acido lattico acqua di Mash pH 5.7 e acqua di sparge pH 5.5.
Le birre sono venute acide… a questo punto non so se per colpa di qualche infezione o se ho acidificato troppo… che ne pensi?
Grazie per la risposta e per i tuoi illuminanti articoli!
Non serve misurare il pH dell’acqua PRIMA di mettere i grani: devi misurarlo e aggiustarlo al valorr giusto DOPO il mash-in. A ogni modo la birra non può risultare acida per l’acido che hai aggiunto con quei valori, probabilmente infezione.
Grazie per le pronte risposte!
Ciao!
Sono un neofita nel mondo della birra fatta in casa e ti faccio i miei complimenti per la tua chiarezza (credo di aver capito anche io!!!)
ti chiedi una precisazione/conferma pratica: inserisco i grandi a 25°C, misuro il PH, eventualmente correggo con acido lattico o similare in base alla scelta di favorire alfo o beta – milasi e poi porto a temperatura target.
Corretto?
Se volessi effettuare una sosta a temperatura proteine – reset (52°c) come dovrei comportarmi per la gestione del PH e temperatura di rilevazione?
Grazie
Corrado
Il pH del mosto va misurato a 20-25°C, ma non è che il mosto in cui sono i grani deve essere a 25°C. Il mash-in (l’inserimento dei grani) lo fai alla temperatura a cui farai il mash (in genere con l’acqua 2-3°C sopra al target, visto che i grani poi fanno scendere leggermente la temperatura). Attendi 10 minuti, prendi un piccolo campione di mosto, lo freddi a 25°C e misuri il pH. Se non va bene, correggi ancora e ripeti.
Grazie mille per l’articolo, chiaro e completo. E’ evidente che hai un talento anche nella didattica.
Sono un neofita e quindi cerco di assorbire più info possibili.
C’è una cosa che non riesco a capire, mi sa che mi sfugge qualcosa di fondamentale. Faccio l’esempio con la proteasi ma vale in generale per le altre fasi. Il range di PH per la proteasi per Palmer è 4.6-5.3 (per Bertinotti 4.6-5.1). Ma se ho regolato il PH per avere il mosto a 5.5 (per esempio) vuol dire che la fase di proteasi sarebbe inefficiente (inutile)?
Parliamo di range di massima, non è che al difuori di quell’intervallo gli enzimi smettono di lavorare all’improvviso. Lo fanno con meo efficienza. Probabilmenteun ph di 5.2
a bene sia per le proteasi che per le amilasi.
Ciao Frank, complimenti ho trovato molto interessante l’articolo, l’ho trovato cercando info sul pH perché ho un problema generico su più ricette e cioè di avere una attenuazione sempre troppo alta (con s-04 per la ultima mia Bitter 80% a 18⁰ stabili) e quindi 3/4 punti sotto la FG target, pur alzando la temperatura di Mash (faccio mono step) a 69⁰, a questo punto ho pensato potesse essere un problema di pH anche perché fino ad’ora non ho mai fatto correzioni, cosa ne pensi potrebbe essere possibile che influenzi a tal punto il lavoro degli alfamilasi?
No, direi improbabile. Molto più probabile una contaminazione di qualche sorta, anche semplicemente di una var Diastaticus (che può essere un semplice lievito belga utilizzato in precedenza, come il French Saison). Dai un’occhiata a questo link: https://brewingbad.com/2019/06/diastaticus-passi-avanti-nella-ricerca/.
Come sanitizzi?
O caspita non avevo proprio pensato a quella eventualità anche perché non ho notato sapori o odori strani, comunque detergo con acqua e sapone e sanitizzo con Sanstar HB su fermentatore inox ora è in precedenza in un keg e anche lì ho avuto lo stesso risultato, sinceramente mi sembrava strano dover aumentare la temperatura di mesh ha 70⁰ per riuscire a estrarre più Alfa che Beta quando le ricette indicavano 67/68.
Per ora ho fatto solo inglesi e ho usato S-04, Dunstar Nottingham, mangrove jack’s yeast m36, White Labs WLP005(su una Porter che per altro è l’unica ad aver centrato la FG)
Non capisco….☹️
Ho letto l’articolo che mi hai segnalato e mi effettivamente potrebbe essere, però io non ho una eccessiva carbonazione in bottiglia, certo é che faccio la carbonazione sempre al valore minimo per lo.stile, bo non saprei…. Cmq una bella disinfettata a tutto gliela dò!