Vivo e produco birra a Roma. Nella mia zona, l’acqua che esce dal rubinetto di casa è particolarmente dura. Per questa ragione, fin dalla prima cotta, ho utilizzato acqua in bottiglia per produrre birra. Nonostante negli anni abbia ridotto i volumi, fino ad arrivare agli attuali 12 litri di birra in fermentatore, mi servono ancora quasi tre casse di acqua per ogni cotta. Tutto questo spreco di plastica non mi è mai andato a genio, ma fino a oggi non avevo avuto tempo né particolare voglia di provare strade alternative.
Tra queste, le più comuni sono pre-bollire l’acqua o utilizzare un impianto di filtrazione a osmosi inversa. Quest’ultimo è sicuramente il metodo più efficace, ma l’impianto costa, va manutenuto e comunque si spreca molta acqua. Essendo costretto a casa in questo assurdo momento storico, l’ipotesi più semplice da percorrere era senza dubbio quella della pre-bollitura.
Ce l’ho dura (l’acqua)
Cosa significa esattamente acqua dura? Partiamo dalla mia acqua di rete per comprendere meglio questo concetto in ottica birraria. Nel mio caso, la rete idrica è gestita da Acea. Sul sito dell’azienda è disponibile una comoda e semplice mappa per recuperare informazioni sull’acqua di rete. Basta inserire il proprio CAP nella piccola casella sopra la mappa di questa pagina per scaricare le analisi dell’acqua aggiornate a Dicembre 2019.
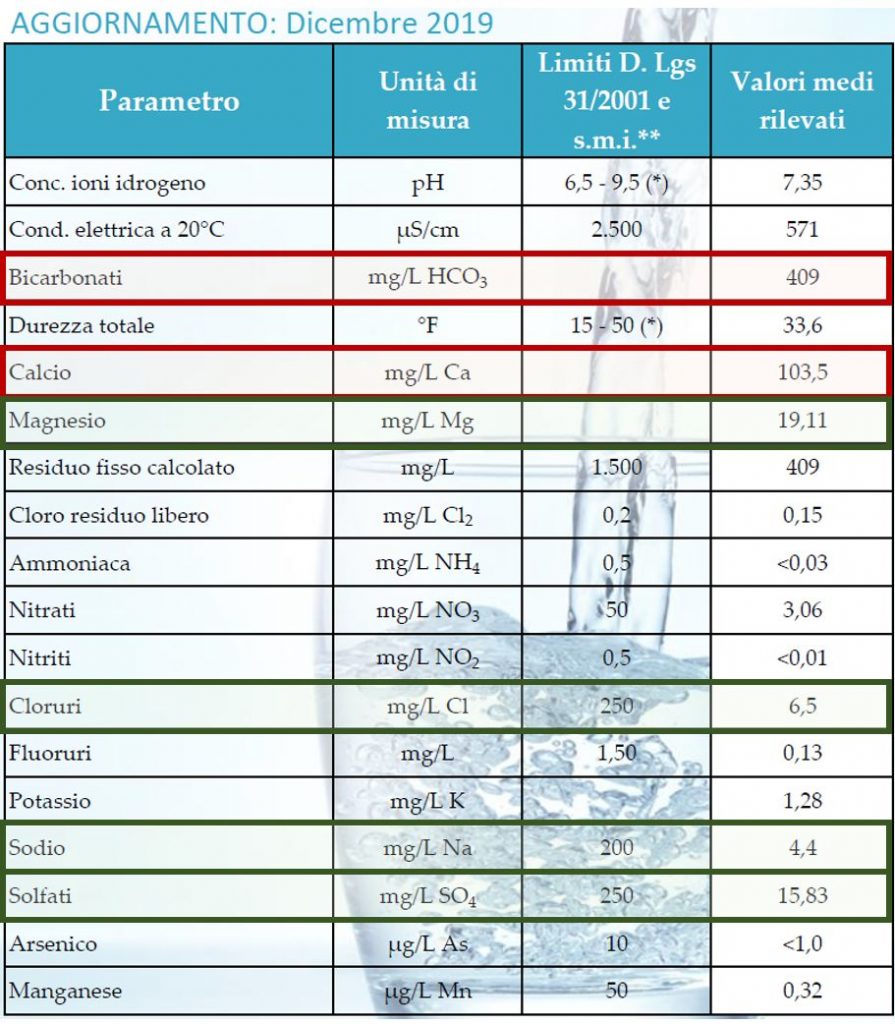
Leggendo attentamente la tabella sopra riportata, notiamo che in realtà nell’acqua solo alcuni sali hanno concentrazioni molto alte, mentre altri sono addirittura scarsi. Nello specifico, bicarbonati (HCO3) e calcio presentano valori piuttosto elevati, mentre la concentrazione di sodio, solfati, cloruri e anche magnesio è assolutamente gestibile.
Calcio e magnesio sono i responsabili della cosiddetta durezza temporanea, mentre solfati e cloruri contribuiscono alla durezza permanente. La differenza tra queste due tipologie di durezza è che la prima si riduce con la bollitura, la seconda invece non si altera se l’acqua viene bollita. Anzi, bollendo a lungo, l’acqua evapora e le ppm (parti per milione o mg/L) di solfati e cloruri tendono ad aumentare.
Ma come fanno calcio e magnesio (soprattutto il calcio, in realtà) a ridursi con la bollitura? Dove vanno? La risposta non è complicata. Questi due ioni, che hanno carica positiva, nell’acqua si legano ad altri ioni con carica negativa. Possono quindi legarsi ai bicarbonati, formando gli idrogenocarbonati. Quando viene applicato calore (sopra gli 80°C) bicarbonati e calcio reagiscono secondo le seguenti equazioni:
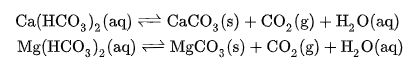
Sembra complicato, ma in realtà è molto semplice: applicando calore si formano carbonato di calcio (calcare, quella patina bianca che si deposita sul fondo della pentola); acqua (H2O), che entra in soluzione; anidride carbonica (CO2), che si libera nell’aria. Dopo qualche minuto di bollitura avremo quindi meno calcio e bicarbonati in soluzione e più calcare sulle pareti della pentola. Anche il magnesio teoricamente prende parte a questa reazione, ma il suo contributo è trascurabile per via della maggiore solubilità in acqua del carbonato di magnesio (si forma ma poi si solubilizza nuovamente).
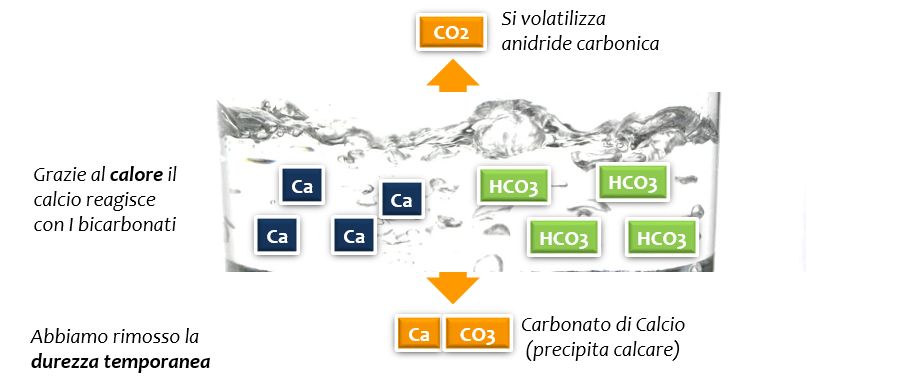
Facendo bollire l’acqua, quindi, possiamo ridurre la durezza temporanea, ovvero abbassare la concentrazione di bicarbonati che è quella che crea maggiori problemi durante il processo di produzione della birra. Di fatto, stiamo abbassando l’alcalinità residua dell’acqua, evitando così che i troppi bicarbonati ostacolino la discesa del pH durante l’ammostamento (qui maggiori dettagli sull’alcalinità residua).
Di quanto si riducono bicarbonati e il calcio? Non è possibile ottenere un numero preciso senza misurare la concentrazione degli ioni nell’acqua bollita, ma per fortuna esistono delle formule approssimative che ci consentono di ottenere una stima ragionevole dei valori finali di calcio e bicarbonati ( si ipotizza che il magnesio non vari significativamente). Martin Brungard, nel suo sito Bru’n Water, utilizza la formula seguente (ppm e mg/L sono la stessa cosa nel caso dell’acqua).
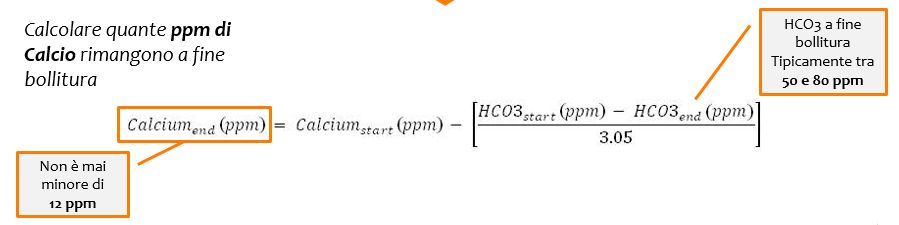
dove:
- Calcium-End = concentrazione del calcio dopo la bollitura (incognita)
- Calcium-Start = concentrazione iniziale del calcio
- HCO3-Start = concentrazione iniziale dei bicarbonati
- HCO3-End = concentrazione finale dei bicarbonati (incognita)
Ovviamente non è possibile risolvere una singola equazione con due incognite, quindi dobbiamo fare delle ipotesi. Brungard ci dice che, in generale, la concentrazione di bicarbonati dopo una bollitura di 10-15 minuti si attesta intorno alle 50-80 ppm. Ci dice anche che, sempre dopo la bolliura, la concentrazione di calcio non scende sotto le 12 ppm.
Non resta quindi che inserire i valori nell’equazione, ipotizzando, ad esempio, una concentrazione di bicarbonati pari al minimo (50 ppm). Se dalla formula otteniamo una concentrazione di calcio maggiore di 12-20 ppm, l’ipotesi delle 50 ppm per i bicarbonati è ragionevolmente corretta. Se invece otteniamo per il calcio un valore troppo basso, si riprova l’equazione alzando la concentrazione di bicarbonati finché non otteniamo un valore superiore alle 12 ppm.
Esempio con la mia acqua di Roma:
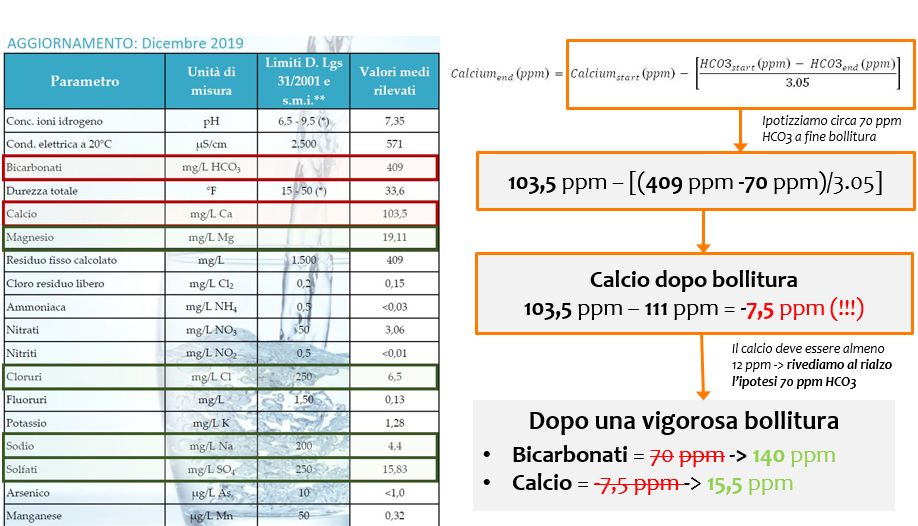
Bollendo l’acqua di Roma otterrò quindi un profilo con 140 ppm di bicarbonati e circa 15 ppm di calcio. Dato che i valori di solfati e cloruri sono bassi, posso aggiungere a questo punto solfato di calcio o cloruro di calcio per riportare il calcio intorno alle 50 ppm (valore ottimale per la fermentazione) bilanciando solfati e cloruri secondo lo stile che andrò a produrre. L’aggiunta di calcio a parità di bicarbonati diminuisce ulteriormente l’alcalinità residua.
Non sto qui ad annoiarvi con altri calcoli ma è interessante notare come, grazie alla pre-bollitura, l’alcalinità residua scende da 247 a 85. Aggiungendo successivamente solfato di calcio e cloruro di calcio per portare il calcio a 50 ppm, l’alcalinità residua scende ulteriormente fino a 50 ppm. Con queste semplici operazioni siamo passati da una alcalinità residua di 247 a 50 ppm.
Una bella riduzione. Servirà molto meno acido per abbassare il pH di ammostamento.
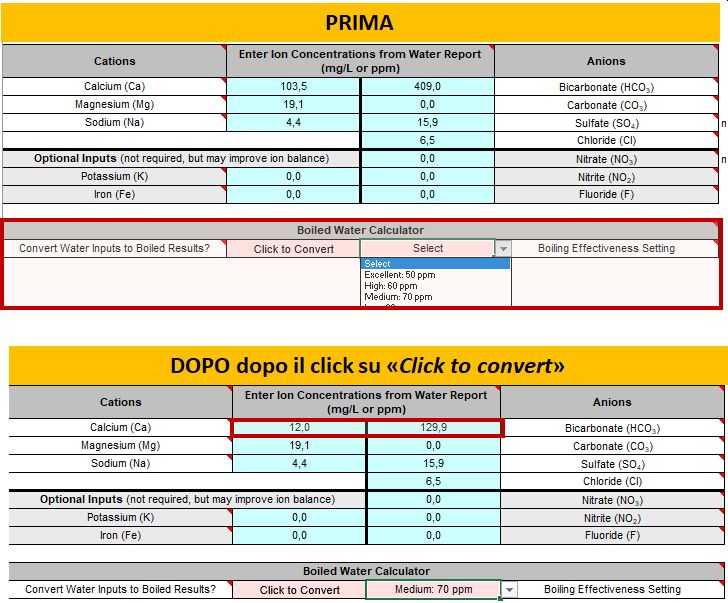
Se non vi va di fare i calcoli a mano, nel file Excel di Bru’n Water, nello sheet “1. Water Report Input”, c’è un pulsantino per lanciare una formula che li fa al posto vostro. Dal menù a tendina si può scegliere l’efficacia della bollitura tra bassa, media o alta. Selezioniamo media per tenerci in un range ragionevole. Come potete vedere nell’immagine sotto, i valori finali sono simili a quelli calcolati con la formula precedente.
[Nota] Per usare le funzioni avanzate del file Brun Water (come questa sulla bollitura dell’acqua) occorre acquistare la versione a pagamento (è sufficiente una donazione di pochi euro che si può fare dal suo sito).
Se non volete usare il file di Bru’n Water, nel tool dell’acqua di Brewer’s Friend potete fare un’operazione molto simile inserendo i valori dell’acqua di partenza nel form Mash Chemistry (link). I valori post bollitura li trovate scendendo in basso fino al TAB “Boiling and Lime Softening”.
Ma non bastava aggiungere acido nel mash?
Ovviamente sì. L’effetto dei bicarbonati nel processo di produzione può essere efficacemente contrastato con l’aggiunta di acido nel mash (lattico, citrico, fosforico).
Ci sta. Potremmo semplicemente aggiungere acido lattico a secchi o usare l’acqua per produrre birre molto scure (avremmo comunque bisogno di un po’ di acido vista la mole di bicarbonati, ma sicuramente meno).
Tuttavia, 400 ppm di bicarbonati, a fronte di sole 100 ppm di calcio, sono troppe. L’alcalinità residua, come abbiamo visto, è molto alta. Per far scendere il pH di ammostamento a valori ragionevoli (5.2-5.5) serve tanto acido. Se si produce una birra chiara, come capita spesso, ne serve ancora di più. Non esiste una concentrazione nota a priori oltre cui un acido inizia ad avere effetti sul profilo organolettico della birra. La percezione nella birra finita dipende da moltissimi fattori come la tipologia di acido, la luppolatura, l’intensità della birra, lo stile di birra e via dicendo. Tuttavia, in genere, meno acido si aggiunge, meglio è. Non lo dico per ragioni di purismo tipo editto di purezza, intendiamoci, ma semplicemente perché nessun acido è completamene insapore e ad alti dosaggi può avere il suo effetto.
Una sola volta ho usato acqua di rete in una cotta, senza prima bollirla ma facendo affidamento sul solo acido lattico per abbassare il pH di mash. Sarà stato un caso, ma la birra che ne è venuta fuori, nonostante avessi raggiunto il pH corretto, aveva decisamente qualcosa che non andava. Non sono stato in grado di capire bene cosa, sinceramente, ma senza dubbio non può essere definita una birra riuscita (vedi recensione della “Yeah I Know” English IPA). 
C’è anche da dire che bollendo l’acqua si ha anche il vantaggio di eliminare il cloro, sempre presente nelle acque della rete idrica, in concentrazioni più o meno alte. Il cloro, legandosi ai polifenoli del malto diventa meno volatile, generando fastidiosi aromi di medicinale (clorofenoli) che permangono nella birra finita.
Purtroppo alcuni gestori idrici usano additivi a base di clorammine, che non sono volatili e non si eliminano con la bollitura. In questo caso si può intervenire con metabisolfito di potassio, ma non ho mai provato. Sul suo sito, Martin Brungard spiega anche questo e indica un dosaggio di circa 8 mg/L di metabisolfito di potassio.
Infine, anche se meno importante, l’acqua bollita è praticamente priva di ossigeno, il che aiuta a ridurre le ossidazioni a caldo (HSA, Hot Side Aeration).
Nella pratica
Bollire l’acqua con cui si andrà a produrre birra è molto più facile a dirsi che a farsi. Nella pratica impegna un bel po’ di tempo, oltre al fatto che bisogna necessariamente farlo prima della produzione, aggiungendo altre operazioni a quelle già impegnative della cotta in sè.
Bisogna fare attenzione perché l’acqua cambia di volume quando viene riscaldata (aumenta di circa un 4%). Se misuriamo il volume dell’acqua calda dopo la bollitura, il giorno dopo ci troveremo con meno acqua rispetto al previsto (in genere l’acqua che si aggiunge per il mash si misura a freddo).
Io ho fatto così. Per prima cosa ho raccolto l’acqua nella pentola di ammostamento, che nel mio caso è più grande di quella di bollitura e ha un rubinetto. Ho misurato un volume (a freddo) leggermente maggiore di quello che mi sarebbe servito per la cotta includendo mash e sparge. Questo perché una parte dell’acqua sarebbe evaporata con la bollitura.
Ho portato quindi a bollitura l’acqua e l’ho lasciata bollire vigorosamente per una decina di minuti. Una volta spento il calore, ho lasciato riposare qualche minuto. Volendo, si può fare un piccolo whirpool per concentrare il calcare nel centro della pentola. Ho quindi iniziato a prelevare l’acqua ancora calda spostandola in un’altra pentola. Non vi preoccupate se vi portate dietro un po’ dei residui calcarei, restano non solubili.
Non mi sono però reso che stavo misurando l’acqua in base al volume occupato a caldo, ragion per cui poi mi sono trovato con un po’ di acqua in meno una volta raffreddata. Ho compensato aggiungendo mezza bottiglia di acqua Panna che avevo in casa.
La pentola in cui ho bollito l’acqua non ne è uscita molto bene.
 Devo dire che non ci ho messo molto a pulirla: 5 litri di acqua tiepida e acido citrico sul fondo (4 g/L), un passata con pezzetta sulle pareti, ammollo della resistenza per una decina di minuti e il gioco è fatto.
Devo dire che non ci ho messo molto a pulirla: 5 litri di acqua tiepida e acido citrico sul fondo (4 g/L), un passata con pezzetta sulle pareti, ammollo della resistenza per una decina di minuti e il gioco è fatto.

Pentola tornata come nuova.

Come è andata la cotta con l’acqua di rete pre-bollita?
Il giorno seguente ho fatto la cotta di una session IPA, utilizzando il profilo modificato dell’acqua e Brun Water per stimare il pH di ammostamento. Ho aggiunto poco più di 3 ml di acido lattico in ammostamento, su un totale di 18 litri di acqua. Il pH è sceso molto vicino a quanto previsto: 5.3 contro i previsti 5.2. Questo mi fa pensare che la stima sulla quantità finale di bicarbonati fosse ragionevolmente corretta.
Ora la birra sta fermentando, quando l’assaggerò aggiornerò anche questo post per valutare il risultato (eccolo! link).
Che dire: un procedimento un po’ laborioso ma utile, in particolare in questo difficile periodo in cui comprare casse di acqua al supermercato è fuori discussione. Non è detto tuttavia che non userò questo metodo anche in futuro, se la birra viene bene. Serve un minimo di tempo in più e si utilizza un po’ di energia (nel mio caso elettricità), ma si risparmiano tante bottiglie di plastica e in finale anche non pochi soldi.






Bellissimo articolo Frank! con un grainfather sarebbe anche molto comodo.
Si può partire con acqua già calda di rubinetto per metterci meno tempo a bollire?
Stavo valutando magari, gestendo bene i tempi, di riuscire a trattenere il calore dell’acqua per poter avere già acqua calda per il mash e per lo sparge, pensi sia una cosa fattibile?
Vero che, in caso di boil nel grainfather, bisogna comunque vuotarlo per pulirlo dal calcare prima della cotta.
Secondo me puoi usare acqua calda, sì. Sulla seconda ti sei risposto da solo 🙂
Te come mai non hai usato acqua calda?
Un po’ perché non ci ho pensato, un po’ perché cmq passa per la caldaia e preferisco non usarla per bere (anche se credo sia ok).
vero, però essendo bollita e poi ribollita nella birra non penso ci siano problemi. si risparmia non poco tempo, solitamente si parte almeno da 50°
Be’, se c’è ferro o qualcosa legato alle tubature non è che la bollitura gli fa nulla. Ripeto, eccesso di zelo, sicuramente.
ah quello no certo, magari son particelle che si depositano e si perdono durante il travaso dell’acqua bollita
Buongiorno, ma cosa succede se l’alcalinità residua prende valori molto negativi?
Nel post trovi il link a un altro post dove è spiegata nel dettaglio l’alcalinità residua e come mai può avere valori negativi.
Il metodo che hai descritto è sicuramente laborioso ma credo che porti ad un livello di controllo del processo e di comodità maggiore alla lunga, se la fornitura idrica è sempre la solita con qualche accortezza si possono risparmiare pure soldi senza rimetterci troppo tempo, preparando tutto 1 giorno o 2 prima di birrificare.
Io abito in collina, non conosco esattamente la composizione della mia acqua di rete ma dalla quantità di carbonati precipitati e dalla misurazione dell’EC prima e dopo la bollitura deduco che sia molto dolce e con concentrazioni di ioni poco (zero!) influenti per la birrificazione (quando metterò le mani sulle analisi avrò un’incognita in meno), partendo da questi presupposti t spiego come faccio io: Utilizzo un filtro brita che si puo attaccare direttamente al rubinetto (brita on tap), così facendo riduco/elimino eventuali metalli pesanti ma soprattutto il cloro (clorammine nn ce nè!), pompo l’acqua in una pentola che contenga tutta quella necessaria al processo, io in genere ne metto almeno 1/3 in più.
Passo poi a bollire l’acqua senza aggiungere prima il calcio (per nn avere troppe incognite e perchè l’acqua me lo consente), dopo una bollitura di 30 minuti necessaria per far compiere
tutto il processo lascio a raffreddare per 24H.
Il giorno della cotta trasferisco (a caduta, o pompa) l’acqua fredda nel mio 3asy50 e misuro precisamente i litri di cui necessito, misuro il ph, aggiungo i sali comportandomi come se avessi acqua osmotica raggiungendo i valori di calcio, solfati e cloruri prefissati (che nn sono mai estremi) e acidifico, nel frattempo pulisco la pentola dai carbonati precipitati e ri-trasferisco tutta l’acqua meno quella che uso nel mash che lascio nell’3asy50 e inizio a scaldare per dare il via alla festa.
Risultato? un po di sbattimenti ma trovo che avere acqua necessaria per tutto il processo compresi sparge, rabbocchi, diluizioni, reidratazioni di lieviti etc etc. sia molto comodo.
E’ meno complicato di quanto sembri
Grazie per il contributo, Zico. PS. cmq non aggiungo calcio durante la pre-bolllitura (forse mi sono espresso male) ma al momento di usare l’acqua per l’ammostamento.
Ciao sono un beginner, sono alla seconda cotta in biap in e+g.
Come già descritto sopra da altri utenti volevo utilizzare l’acqua della rete idrica,(abito in prov di Venezia e di solito uso la San Benedetto!) anche io ma per fare un e+g. Avendo le materie prime Estratto liquido e in polvere più grani Crystal, se non ho capito male dai libri e post letti non dovrebbe essere necessaria la correzione del ph.
Confermi Frank ? Grazie in anticipo
Hai letto bene, vai tranquillo!
Questo è quello che si dice un consiglio semplice ma efficace, grazie!
Ho sempre problemi di ph troppo alto, il ph stabilizer 5.2 mi porta l’acqua a 6.2/6.3 con le dosi consigliate e non mi va di eccedere.
Cosa ne pensi di questo prodotto? Se non altro organoletticamente non da alcun gusto alla birra
Per il cloro ho sempre “impentolato” l’acqua mash e sparge la sera prima e lasciata evaporare, chissà se basta…
Non ho mai usato il pH stabilizer ma non mi piace l’idea. A parte che il valore a cui porta l’acqua PRIMA del mash non conta nulla (dipende quanti bicarbonati rimangono) il punto è che va inevitabilmente a modificare il profilo dell’acqua in modo non noto. A quel punto perde un po’ di senso andarsi a calcolare eventuali aggiunte di sali. Meglio usare acido.
Verissimo, la bollitura dell’acqua è uno dei metodi che può essere adottato per ridurre il livello di pH dell’acqua. Sconsiglio vivamente l’utilizzo di acqua calda (dalla caldaia) perchè solitamente vengono applicati in ingresso dei dosatori di polimeri (la polverina che limita il legame molecolare tra calcio e magnesio). Far bollire l’acqua di rete porta all’evaporazione dei trialometani presenti nell’acqua in relazione al cloro (ipoclorito di sodio) che ne garantisce la riduzione della carica batterica. La temperatura alta rompe dei legami molecolari e ne facilita altri non sempre auspicabili. Buon lavoro
Grazie!
non ho capito, sconsigli l’uso di acqua calda di rete, ma sempre la stessa acqua, che non è passata dalla caldaia di casa?
Le caldaie spesso hanno un piccolo contenitore che aggiunge polisfosfati all’acqua per abbattere il calcio, quindi meglio non usarla per birrificare. Poi se la caldaia è centralizzata al palazzo o solo nell’appartamento non cambia. Meglio non usare l’acqua calda, ma partire da quella fredda.
Ciao Frank complimenti per il blog anche perché mi ritrovo spesso nella tua idea di semplificare al massimo tutte le fasi di produzione e di farsi meno seghe mentali…
Tornando al tema del post,purtroppo le condizioni della mia acqua di rete sono pessime, non sempre riesco ad usare acqua in bottiglia più che altro per comodità,sicuramente proverò a seguire i tuoi consigli per abbassare calcio e bicarbonati bollendola,però ho anche il problema dei solfati,di seguito ti indico i valori della mia acqua se puoi darmi un consiglio su come tratteresti la stessa per renderla utilizzabile non dico per le pilsener ma almeno per un range abbastanza vario di stili….grazie Yury
Bicarbonati 307
Calcio 191
Cloruro 40
Magnesio 25
Solfati 260
Sodio 25
Ahimè per i solfati l’unica strada è diluirla oppure osmosi inversa, non c’è molto altro da fare.
Come pensavo grazie della risposta…
Per quanto riguarda le birre luppolate come ipa oppure birre scure se ho letto bene il valore dei solfati deve essere alto,giusto?
https://brewingbad.com/2015/12/i-profili-delle-acque-storiche-sono-una-bufala/. 🙂 però nel tuo caso puoi provare, non avendo alternative…
Ciao Francesco! Posso usare l’acqua del rubinetto anche se addolcita? Temo che l’aumento del NA vada ad danneggiare i saccarom. Grazie per l’articolo interessante
L’acqua addolcita è un problema per la produzione di birra, come ipotizzi anche tu. Non necessariamente per la salute del lievito, che pure ha difficoltà a fermentare oltre un tot di concentrazione di sodio, ma per il fatto che si sente proprio il salato quando la bevi. Non la userei, ma bisognerebbe capire la concentrazione di sodio (ma se usi l’addolcitore è probabile che l’acqua di partenza sia molto dura e quindi l’addolcitore aggiunge parecchio sodio).
Ciao Frank, mi hai fatto venir voglia di cercare le analisi della mia acqua!
mi sono trovato questi valori:
Bicarbonati 238 mg/L
Calcio 50,5 mg/L
Cloruri 9 mg/l
Magnesio 25,5 mg/L
Sodio 7,5 mg/L
Solfati 26 mg/L
nel mio caso ha senso bollire l’acqua? Perchè i valori di Cloruri e Solfati (responsabili di durezza permanente) sono più elevati.
Come valuti l’uso dei prodotti Stabilizzatori Ph a 5,2 (credo che siano dei sistemi tampone)?
Grazie!
Ciao Alberto! Dunque, se la tua acqua va bene oppure no puoi valutarlo da solo con i tool segnalati nel post (tra l’altro solfati e cloruri non sono affatto alti). La risposta alla seconda domanda è invece quattro commenti più sopra. 🙂
…hai ragione perdonami ☺ usando il foglio di calcolo EZ Water Calculator (quello di Bru’n Water non riesco ad aprirlo con open office):
con il grist della prossima cotta (Berliner Weisse) mi vine fuori un Ph di 6,15.
Purtroppo non ho disponibili acido lattico per correggere (ne servirebbero 8ml). É possibile usare in qualche modo il succo di limone? O altro facilmente reperibile in casa?
Facilmente reperibile in casa solo il succo di limone, ma il problema è che aggiunge anche la parte di sapore e non ho idea di quanto ne serva. Puoi provare.
oppure ho del Gypsum comprato tempo fa però ne servirebbero 50g e mi sparano su i valori di calcio e solfati
Non mi pare una strada percorribile.
Ciao Frank, complimenti per l’articolo.
Ho provato a bollire l’acqua per circa 20 min e, ora che si è raffreddata, oltre ad avere i precipitati sul fondo, mi ritrovo anche delle particelle in sospensione (tipo pagliuzze trasparenti)… È normale? Si tratta di carbonato di calcio non precipitato?
Ciao Emanuele: “precipitato” non significa necessariamente che lo trovi sul fondo o sulle pareti, ma che è uscito dalla soluzione. Quindi può anche galleggiare, sì.
Perche non tagliarla con acqua distillata?
Perchè l’acqua distillata che si compra al supermercato nella maggior parte dei casi non è potabile
Cosa rende o meno l’acqua potabile? Dovresti saperlo bene tu.
L’acqua distillata venduta nei boccioni da 5 litri nel supermercato è data come “priva di purezza batteriologica a causa del sistema di produzione” quindi dove la fanno non stanno tanto a guardare alla sanificazione degli impianti.
Portandola in bollitura però durante il procedimento (per almeno un’ora con birre tradizionali) direi che la purezza batteriologia la fai tu tranquillamente.
Valuta..
Ciau
Non è proprio così, ci possono essere altri resodui di produzione inorganici (oli minerali, metalli etc) che non elimini con la bollituta. Spesso c’è scritto “non adatta al consumo alimentare” e bollirla non risolve interamente il problema. Dipende ovviamente dalle tipologie, ma non generalizzerei (su quella che ho davanti ora e uso per il ferro da stiro c’è scritto per esempio “tenere fuori dalla portata dei bambini)
Interessantissimo articolo Frank, ho sempre saputo della bollitura come soluzione ad un acqua troppo dura ma non mi sono mai addentrato nei calcoli e nella pratica di come affrontarla.
L’ acqua del mio comune è pressappoco identica alla tua, solo che la cosa che mi scoraggia a procedere con la bollitura è la quantità di acqua e la conseguente perdita di tempo dato che produco circa 80 litri a cotta. E poi mi sorge il dubbio di cosa fare con l’acqua di sparge. Dovrei bollire anche quella per avere la stessa fonte che ho nel mash o posso farne a meno, considerando che i bicarbonati non mi daranno più problemi e non influiscono sul sapore. In base alle tue risposte valuterò cosa mi conviene fare per le prossime cotte.
I bicarbonati sono cmq un problema anche nell’acqua di sparge, perchè devi portarla a ph 5-5.5 e l’unico modo per farlo senza bollire sarebbe aggiungere quintalate di acido. Puoi provare (sarà sempre in quantità minore in totale rispetto a non bollire nemmeno l’acqua di mash) ma io a questo punto bollirei tutto. Ma chi te lo fa fare a produrre 80 litri a cotta! 🙂
Per te che hai sempre odiato lo sbattimento e scelto sempre la via più breve, tutta sta roba mi sembra un bello sbattimento, poi, se uno ha all in one come in tanti hanno, diventa lunga.
Comunque sempre mitico ciao Frank..
Si, vero: gran sbattimento. Però con il fatto che non possiamo uscire il weekend, il sabato faccio bollire mentre faccio altro, e domenica faccio cotta. Non so se avrò tempo per fare tutte queste cose quando (speriamo presto) si ritornerà alla normalità.
Ciao Frank, oltre ad abbattere la durezza temporanea, ravvedi anche qualche beneficio per quanto riguarda la limitazione di precursori di ossidazione in fase di mash?
Difficile valutarlo con due sole prove, tra l’altro entrambe IPA con vagonate di luppolo.
Articolo molto interessante, me lo ero perso. Qualche anno fa mi ero fissato con l’acqua. Rivedo in questo articolo tanti punti che mi assillavano. La mia birra aveva sempre uno strano amaro e cambiava di sapore velocemente. Tantissime prove simili alle tue Franck, ma alla fine ho optato per un “vigliacco”, ma buon, impianto ad osmosi. 🙂
Ciao Frank, articolo molto dettagliato ed istruttivo! Dopo aver letto il tuo articolo, sto pensando di provare se ci sono differenze sui lievitati (impasti per pizze, pane, etc.). Normalmente uso acqua in bottiglia, che mi assicura caratteristiche stabili e niente cloro.
Potrei provare due impasti, uno con acqua di rubinetto senza bollitura, ed un impasto con acqua dopo la bollitura. Ottenere acqua con pH tra 5 e 6, senza cloro, sarebbe l´ideale.
KH (durezza temporanea) si abbassa, come spieghi bene, mentre GH (durezza totale) dovrebbe aumentare di poco, per effetto di evaporazione, confermi?
Ho trovato delle pagine in cui si dice che acqua dopo bollitura acquista un pH alcalino, può dipendere dal valore pH di partenza?? https://www.virya.com/alcalinizziamo-nostro-corpo/
Grazie!
Per esperienza (misura diretta) posso confermarti che il pH dopo la bollitura sale. Ma il suo valore assoluto nella produzione della birra è poco importante, quello che conta è l’alcalinità (la resistenza alla discesa del pH) che invece scende notevolmente. Per la pizza non so. La durezza totale dovrebbe comunque scendere, perché è somma di quella temporanea (che scende molto) e quella permanente (che sale di poco).
Ciao, prima di tutto complimenti non solo per questo articolo ma in generale per tutto il lavoro ricerca e sperimentazione che fai. Ritornando all’acqua io nel report dell’acqua del mio comune non trovo i valori di CO3 e HCO3, c’è qualche formula per poterli ricavare dagli altri?
GRAZIE Stefano
La concentrazione di CO3 (carbonati) è trascurabile al pH dell’acqua potabile (in genere tra 7 e 8,5). Quella di HCO3 puoi ricavarla in modo approssimativo moltiplicando la durezza in gradi francesi (quella dovresti averla) per 10. È un’approssimazione, ma in assenza di altro…
Fatto, sono 19 gradi francesi, Grazie ancora.
Ciao Frank, tempo fa ho seguito un video di altri homebrewer in cui parlavano del trattamento dell’acqua con latte di calce per ridurre l’alcalinità. Sto sperimentando il processo e devo dire che è abbastanza veloce e semplice. Mi piacerebbe riuscire a “calcolare” le quantità di calcio magnesio ecc. ma non saprei da dove partire. Sarebbe interessante un tuo articolo su questo processo.
Si può fare, ma è piuttosto complicato calcolare i valori post modifica. Di fatto, da quello che ho capito, la calce spenta fa precipitare carbonato di calcio riducendo calcio e bicarbonati, esattamente come la bollitura. Solo che poi non è facile stimare la concentrazione dei sali nell’acqua post modifica. Inoltre, non mi è chiaro se la calce spenta che si trova ad esempio su amazon sia per uso alimentare (in genere viene usata per concimare il terreno, non per scioglierla nell’acqua che poi si beve). A questo link trovi anche un foglio di calcolo che si può usare per stimare i valori dell’acqua dopo il trattamento, ma lo trovo piuttosto complesso e poco intuitivo. La bollitura mi sembra molto più semplice anche se ovviamente ci vuole più tempo:
http://braukaiser.com/wiki/index.php/Alkalinity_reduction_with_slaked_lime
Ciao Frank, ho provato a seguire le tue indicazioni e sono andato a misurare il ph pre e post Boil ( dopo aver rimosso con un colino tutta la zella). Ora ti chiedo visto che la bollitura dovrebbe comportare un’aggiunta inferiore di acido lattico per correggere il ph, come mai da un ph preboil di 6.8 mi ritrovo un ph 8 post boil?
Grazie
Il pH in sè nin ti dà indicaziobi sull’alcalinità residua (ovvero ma la cobcentrazione di bucarbobati) che sarà sicuramente diminuita con la bollitura. Ti servirà infatti meno acido lattico per far scendere quel pH di 8 a 5.2 nel mash rispetto a quanto te ne sarebbe servito per farlo scendere da 6.8 a 5.2 senza aver prebollito l’acqua.
Tutto chiaro! Grazie mille per le tue pronte risposte
Ciao Frank. All’inizio dell’ultima cotta ho pre-bollito l’acqua per 15 minuti e poi l’ho raffreddata con il chiller controflusso alla temperatura di mash-in e poi sono partito con l’ammostamento come al solito. Ho fatto questo per ridurre al minimo l’ossigeno disciolto nell’acqua e limitare così l’ossidazione a caldo (www.themodernbrewhouse.com). Non avendo fatto raffreddare lentamente l’acqua e depositare i composti generati dalla bollitura, immagino che bicarbonati e calcio siano rimasti gli stessi dell’acqua di partenza o li ho comunque ridotti in bollitura?
Seconda domanda: facendo un mash in 2 step, mi sono chiesto perchè il primo step di mash deve essere sempre ad una temperatura inferiore rispetto al secondo step? In questo caso a me sarebbe convenuto fare viceversa, prima mash-in alla temperatura alta del secondo step e poi lasciare raffreddare fino alla temperatura del primo step per poi tornare su con il mash-out. In pratica avrei fatto lavorare prima gli enzimi alfa-amilasi e poi beta-amilasi. E’ giusto o mi sfugge qualche altra implicazione? Grazie come sempre!
Nel caso dell’acqua, bollire 15 minuti potrebbe non essere particolarmente incisivo. Il raffreddamento veloce non credo c’entri e non credo nemmeno serva a granchè in termini di riduzione dell’assorbimento di ossigeno nell’acqua di mash e sparge. Che comunque è un problema – ammesso che lo sia – assolutamente secondario nel processo di produzione (lascia stare quel sito, è gestito da un “estremista” dell’ossigeno a cui non darei sinceramente troppo credito). Per quanto riguarda gli enzimi, la risposta è abbastanza semplice: tendono a denaturarsi velocemente se sottoposti a temperature più alte rispetto al loro range di funzionamento. Se parti alto e scendi, è probabile che quando arrivi in zona beta-amilasi siano rimasti pochi enzimi in grado di lavorare, con conseguente impatto su tempi e efficienza di conversione.
Concordo sul LODO-estremismo di quel sito 🙂
Ho pensato fosse interessante bollire subito prima del mash, anzichè il giorno prima, perchè così l’acqua l’ho scaldata una volta sola risparmiando un pò di corrente. Inoltre l’acqua usata nel controflusso per raffreddare quella di mash, l’ho messa nel bollitore dello sparge, così sono partito con un’acqua già calda anche per lo sparge, risparmiando ancora un pò di energia ed evitando di sprecare acqua. Poi, oltre a ridurre alcalinità e ossigeno disciolto, ho pensato che fosse utile anche per far evaporare cloro e suoi derivati. Dici che questo modo non è molto incisivo perchè non ho lasciato decantare i sedimenti con un lento raffreddamento o perchè avrei dovuto far bollire per più tempo?
Per le temperature del mash sei stato chiarissimo 🙂
Grazie
Non ho certezze sui tempi di bollitura necessari per far precipitare tutto il carbonato di calcio possibile (non potendo misurare), ma io in genere mi tengo sulla mezz’ora. Ma possibile che anche 15 minuti siano sufficienti (anche per far evaporare il cloro).